Sinopharm (Peking): BBIBP-CorV
1. FÁZIS
1 Próba
ChiCTR2000032459
Kína
2. FÁZIS
2 próba
NCT04962906
Argentína
ChiCTR2000032459
Kína
3. FÁZIS
6 próba
NCT04984408
ChiCTR2000034780
Egyesült Arab Emírségek
NCT04612972
Peru
NCT04510207
Bahrein, Egyiptom, Jordánia, Egyesült Arab Emírségek
NCT04560881, BIBP2020003AR
Argentína
NCT04917523
Egyesült Arab Emírségek
Jóváhagyások
A WHO sürgősségi felhasználási listája 59 Országok
Angola, Argentína, Bahrein, Banglades, Fehéroroszország, Belize, Bolívia (többnemzetiségű állam), Brazília, Brunei Darussalam, Kambodzsa, Kamerun, Csád, Kína, Comore -szigetek, Egyiptom, Egyenlítői -Guinea, Gabon, Gambia, Georgia, Guyana 、 Irán (Iszlám Köztársaság), Irak, Jordánia, Kirgizisztán, Laoszi Népi Demokratikus Köztársaság
Libanon, Malajzia, Maldív -szigetek, Mauritánia, Auritius, Mongólia, Montenegró, Marokkó, Mozambik, Namíbia, Nepál, Niger, Észak -Macedónia, Pakisztán, Paraguay, Peru, Fülöp -szigetek, Kongói Köztársaság, Szenegál, Szolézia, Szerbia Szigetek, Szomália, Sri Lanka, Thaiföld, Trinidad és Tobago, Tunézia, Egyesült Arab Emírségek, Venezuela (Bolivári Köztársaság), Vietnám, Zimbabwe
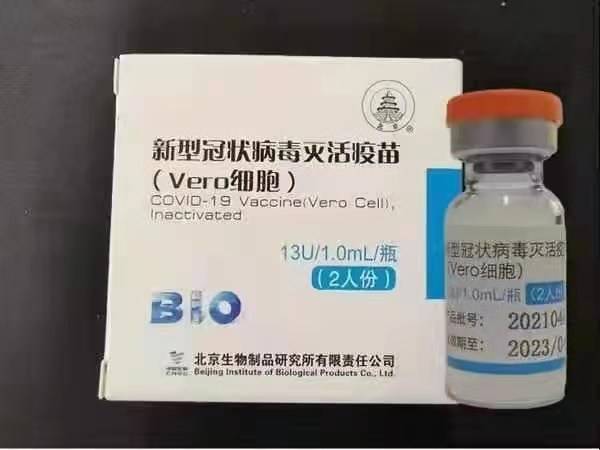
A Sinopharm BBIBP-CorV COVID-19 egy inaktivált vakcina, amelyet tenyésztett vírusrészecskékből állítanak elő, amelyek nem rendelkeznek patogén képességgel. Ezt a vakcinajelöltet a Sinopharm Holdings és a Pekingi Biológiai Termékek Intézete fejlesztette ki.
A Sinopharm BBIBP-CorV vakcina úgy működik, hogy lehetővé teszi az immunrendszer számára, hogy antitesteket termeljen a SARS-CoV-2 béta koronavírus ellen. Az inaktivált vírusvakcinákat évtizedek óta használják, mint például a veszettség elleni védőoltást és a hepatitisz A védőoltást. Ezt a fejlesztési technológiát sikeresen alkalmazták számos jól ismert vakcinára, például a veszettség elleni oltásra.
A Sinopharm SARS-CoV-2 törzsét (WIV04 törzs és MN996528 könyvtári szám) izoláltuk egy páciensből a kínai Vuhant-i Jinyintan Kórházban. A vírust kultúrában szaporítottuk kompetens Vero sejtvonalban, és a fertőzött sejtek felülúszóját β-propiolaktonnal (1: 4000 térfogat/térfogat, 2-8 ° C) inaktiváltuk 48 órán keresztül. A sejtmaradványok tisztázása és az ultraszűrés után egy második β-propiolakton inaktiválást végeztünk ugyanazokkal a feltételekkel, mint az első inaktiválást. A WHO szerint a vakcinát 0,5 mg timsóra adszorbeálták, és előretöltött fecskendőkbe töltötték 0,5 ml steril foszfátpufferolt sóoldatban tartósítószerek nélkül.
2020. december 31 -én az Állami Gyógyszerügyi Hivatal bejelentette a Sinopharm által kifejlesztett kísérleti vakcina jóváhagyását.
2021. május 7 -én az Egészségügyi Világszervezet bejelentette a vakcina jóváhagyását. A WHO sürgősségi felhasználási listája lehetővé tette az országok számára, hogy meggyorsítsák saját hatósági engedélyeiket a COVID-19 vakcina behozatalára és beadására. A WHO immunizációs stratégiákkal foglalkozó tanácsadó szakértői csoportja is befejezte a vakcina felülvizsgálatát. A rendelkezésre álló bizonyítékok alapján a WHO két adag oltást javasol, három -négy hét különbséggel, 18 éves és idősebb felnőttek számára. A védőoltás hatékonysága a tüneti és kórházi kórképekkel szemben 79%, minden korcsoportban együttvéve.
Az Amerikai Orvosi Szövetség 2021. május 26-án közzétette "Randomizált klinikai vizsgálat: 2 inaktivált SARS-CoV-2 vakcina hatása a tüneti COVID-19 fertőzésre felnőtteknél", arra a következtetésre jutva, hogy "ebben a randomizált klinikai vizsgálat előre meghatározott időközi elemzésében, felnőttek A randomizált klinikai vizsgálatok ezen előre meghatározott időközi elemzésében beadott 2 inaktivált SARS-CoV-2 vakcina jelentősen csökkentette a tüneti COVID-19 kockázatát, és súlyos mellékhatások ritkák voltak. " Ebben a 3. fázisú, felnőtteken végzett randomizált vizsgálatban a 2 inaktivált teljes vírus elleni vakcina hatékonysága tüneti COVID-19 esetekben 72,8%, illetve 78,1% volt. 2 vakcinának ritka súlyos mellékhatása volt, hasonló gyakorisággal, mint a csak timsó-kontroll csoport, és a legtöbb nem kapcsolódott az oltáshoz. Egy feltáró elemzés megállapította, hogy a 2 vakcina mérhető semlegesítő antitesteket indukált, hasonlóan a 1/2 fázisú vizsgálat eredményeihez.
A WHO SAGE munkacsoportja 2021. május 10-én közzétette a Sinopharm/BBIBP COVID-19 vakcina áttekintését. A GAVI COVID-19 elleni oltása tartalmaz egy oltóanyag fiolával ellátott monitort, amely tájékoztatja az egészségügyi dolgozókat arról, hogy a vakcinát megfelelően tárolták-e, és túlmelegedés. Ennek eredményeként a károkról a GAVI 2021. május 14 -én számolt be. A Zebra Technologies által gyártott és a Temptime Corporation által készített intelligens címkék egy körből állnak, közepén világosabb színű négyzettel, színtelen vegyi anyagból, amely visszafordíthatatlanul kifejti a színt az idő múlásával. . Ez sötétebbé válik, hogy vizuálisan jelezze az összesített hőhatást. Amint az injekciós üveget az optimális tárolási tartományon túli hőnek tették ki, a négyzet sötétebb lesz, mint a kör, ami azt jelzi, hogy a vakcinát nem szabad tovább használni.
Nemzeti kábítószer-BBIBP-CorV COVID-19 vakcina gyógyszerkönyvtár nyilvántartási száma: DB15807.